En la industria de procesado alimentario es importante verificar las concentraciones correctas de detergentes y desinfectantes. Las concentraciones adecuadas no sólo son necesarias para limpiar y desinfectar correctamente, sino también para asegurar que el proceso se realiza a coste óptimo. Hay varios métodos para medir las concentraciones de las soluciones. En situaciones específicas, varios de estos métodos se pueden combinar para proporcionar información de apoyo adicional acerca de las concentraciones químicas.
 pH
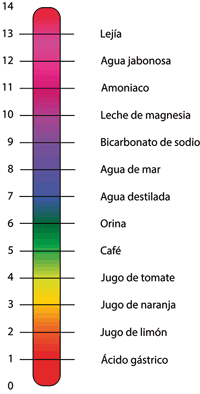
pHEn química, el pH es la medida del carácter ácido o básico de la solución (términos más familiares pueden ser ácidos y cáusticos). Una escala de pH va de 0 a 14. Las soluciones con un pH de menos de 7 son ácidos y las soluciones con un pH mayor de 7 son básicas o alcalinas. La escala de pH no es lineal, sino más bien logarítmica. Cada valor entero de pH por debajo de 7 es diez veces más ácido que el siguiente valor más alto. Por ejemplo, un pH de 4 es diez veces más ácido que un pH 5 y 100 (10 x 10) veces más ácido que un pH 6. Lo mismo sucede para el pH por encima de 7, cada uno de los cuales es diez veces más alcalino que el siguiente valor entero inferior. Por ejemplo, pH 10 es diez veces más alcalino que el pH 9 y 100 veces (10 x 10) más alcalino que pH 8.
El pH es un componente importante en el proceso de limpieza y desinfección:
- • Detergentes: Las suciedades de diferentes tipos se retiran a niveles de pH específicos. Las grasas y los aceites, por ejemplo, se eliminan mejor cuanto más alcalina es la solución de limpieza. Los minerales, por otra parte, se eliminan más fácilmente cuanto más ácida sea la solución.
- • Desinfectantes: En la mayoría de los casos, Los microorganismos son sensibles al pH del entorno. Un cambio drástico en el pH hará que el organismo ya no pueda funcionar y muera. Muchos desinfectantes pueden usar el pH para contribuir a la eficacia del mismo. Pero el uso de nivel de pH para medir las concentraciones no es un método eficaz. El pH ayuda a entender el grado de acidez o alcalinidad de una solución, pero no proporciona una concentración precisa. Los métodos para la medición de pH pueden ser costosos y requieren de calibración, como medidores de pH. Las sondas de pH pueden ser de vidrio, material que no debe ser usado en entornos de producción de alimentos. Las tiras de papel de pH proporcionan una indicación básica de pH.
La conductividad
La conductividad eléctrica es la medida de la capacidad de un material específico para conducir corriente eléctrica. Cabe destacar que el agua pura no puede conducir la electricidad. Son los elementos que se encuentran en el agua los que conducen la electricidad. En comparación con el pH, la conductividad tiene un comportamiento más lineal. Este comportamiento lineal lo convierte en una mejor herramienta de medición para las concentraciones químicas.
 La conductividad tiene sus límites
La conductividad tiene sus límitesLa conductividad tiene algunos problemas. Las sondas de conductividad deben ser limpiadas y calibradas periódicamente. Si el carácter iónico del agua suministrada usada como base cambia, la conductividad general puede subir o bajar. Aunque la conductividad sea una buena herramienta para medir las concentraciones, no debería ser el único método usado. Hay situaciones en las que la conductividad puede ser inexacta. La neutralización puede ocurrir cuando se mezclan ácidos y bases (alcalinos). Cuando se mezclan, se forman sales. Las sales son grandes conductores, pero no son buenos limpiadores. Las sales se mostrarán claramente en medidores de conductividad. Por ejemplo, la mayoría de las plantas de bebidas y cerveceras utilizan CO2 en el proceso de fabricación. Si el CO2 no se purga correctamente en el equipo de procesamiento, antes de la fase de limpieza, el CO2 se disolverá en la solución como ácido carbónico y neutralizará los limpiadores alcalinos para formar sales de carbonato. Las sales de carbonato no son buenos limpiadores pero aparecen claramente en el equipo de conductividad.
Valoración o titulación química
La palabra titulación viene de la palabra latina titulus, que significa inscripción o título. La palabra francesa titre, con el mismo origen, significa rango. La titulación, por definición, es la determinación de rango o concentración de una solución con respecto al agua con un pH de 7 (que es el pH del agua destilada en condiciones estándar). El punto final es el punto en el que finaliza la valoración, según un indicador determinado. En la mayoría de los casos, el indicador produce un cambio de color alrededor del punto (final) de equivalencia de la valoración.
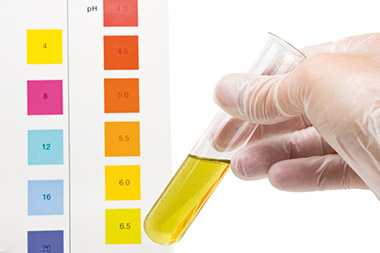
En la valoración clásica de un ácido fuerte usando una solución conocida de valorante base, el punto final de una valoración es el punto en el que el pH de la sustancia reactiva es casi igual a 7 (ver figura). En este caso, el indicador es transparente e incoloro en condiciones ácidas y de color rosa en condiciones alcalinas. Mediante la adición de una concentración conocida de valorante alcalino, el pH de la solución va de un pH ácido (menos de 7) a un pH neutro.
El punto final es cuando la solución se vuelve de color rosa. Debido a la naturaleza logarítmica de la curva de pH, las transiciones son, en general, extremadamente rápidas; y, por lo tanto, una sola gota de valorante justo antes del punto final puede cambiar el pH significativamente, lo que conduce a un cambio de color inmediato en el indicador. Los Kits de prueba de Diversey utilizan botellas con cuentagotas para medir la cantidad de reactivo añadido. El recuento de gotas se multiplica con un Factor de Ajuste de prueba (número de gotas de solución valorante x Test Set Factor). El resultado es la concentración, y dicha concentración puede expresarse de diferentes maneras.
¿Cuáles son las diferentes formas de expresar la concentración?
La concentración de un detergente o desinfectante se puede expresar de muchas maneras y merece alguna explicación. Los detergentes y desinfectantes químicos no son normalmente soluciones químicas individuales; se trata de mezclas de sustancias químicas que hacen que un producto sea adecuado para limpiar suciedades específicas. Los cáusticos, los ácidos, los agentes tensioactivos, los secuestrantes de agua, los disolventes, etc. son sólo algunos de los componentes utilizados en la fabricación de detergentes y desinfectantes. Cuando realizamos la valoración de una mezcla química nos centramos en uno de los componentes de ese producto, que se llama el analito. En este caso el analito podría ser el cáustico, el ácido, el cloro, o cualquier componente que tiene un punto final de valoración nítido. La concentración puede expresarse de muchas maneras. A continuación se presentan ejemplos comunes.
- - ppm - partes por millón: partes por millón se utiliza para denotar proporciones relativas. Si usted tiene una solución que es de 200 ppm de cloro, significa que hay 200 gramos de moléculas Cl2 por cada millón gramos de moléculas de H2O. Por lo tanto ppm es una cantidad adimensional.
- - v / v - volumen por volumen: esto indica un volumen de valor de volumen y por lo general se expresa como un porcentaje. Por ejemplo, una solución v / v de etanol 40 % contiene 40 ml de etanol por 100 ml de volumen total.
%2010.12.44.png) - mL / L - mililitros por litro: este es otro tipo de valor de volumen por volumen usando el sistema métrico de mililitros y litros. Es mucho más fácil entender las concentraciones de métricas porque todas las unidades son con base 10. Una solución de 3 ml / l es lo mismo que una solución de 0,30 % v / v.
- mL / L - mililitros por litro: este es otro tipo de valor de volumen por volumen usando el sistema métrico de mililitros y litros. Es mucho más fácil entender las concentraciones de métricas porque todas las unidades son con base 10. Una solución de 3 ml / l es lo mismo que una solución de 0,30 % v / v.- - w / w - peso a peso: Esto se llama valor de peso por peso y se expresa generalmente como un porcentaje.
- TAREA
- 1.QUÉ HARÁ SI UD FUERA UN Ingeniero en biotecnología, . ESCRIBA TRES COSAS Y LA RAZÓN PORQUE LO HARÍA
- EN UN A HOJA PERFORADA REALICE UN MAPA CONCEPTUAL DE LA PAGINA 197 DE LA FORMA ADECUADA SOBRE CONCENTRACIONES QUÍMICAS.
- 3. RECUERDE SI NO ES NECESARIO SALIR. "QUÉDESE EN CASA"
No hay comentarios:
Publicar un comentario