domingo, 23 de noviembre de 2014
COMBUSTIBLE EN BASE A LA CAÑA DE AZUCAR (CLUBES)
Análisis de dos casos de estudio
Si se toman dos casos de estudio de producción diversificada, el primero con producción de azúcar y de etanol a partir de miel final, y el segundo, con producción de azúcar y de etanol a partir de miel B y jugo de los filtros, tendremos como resultados los mostrados en los esquemas de las figuras 3 y 4, obtenidos en corridas del programa DAFLEX (Diversificación Azucarera Flexible) desarrollado en el ICIDCA sobre hoja de cálculo EXCEL [Díaz, et al., 2002]. Los esquemas anteriores se calcularon tomando como base los parámetros que se muestran en la tabla II.
Del análisis de ambos esquemas, y de los parámetros de operación de la tabla 2, se observa que las diferencias entre la energía eléctrica generada durante y después de zafra, así como en la energía consumida en los procesos de producción de azúcar y etanol, no son muy grandes; el segundo esquema (Fig. 4) vende 4,64 MWh más durante ambas etapas, que el primero (Fig. 3), en el que resulta mayor la electricidad vendida después de zafra (16,95 MWh), generada con el bagazo sobrante que se emplearía en la producción de etanol, si no se utilizara en la generación de electricidad. Por tanto, partiendo de una producción de 186 L de etanol por tonelada de bagazo con los procesos actuales de hidrólisis de biomasa, se simuló la generación de electricidad a partir del etanol obtenido con el bagazo sobrante en los dos esquemas anteriores, con las mismas condiciones de ambos, y que se presentan en las figuras 5 y 6, donde se observa que la cantidad de etanol producido en ambos esquemas se diferencia sólo en 2,24 t/día, que representan alrededor de 2 835 L de etanol más por día, pero la electricidad que se produce en ambos casos no difiere y es de 4,70 MWh.
En este caso, si se compara la electricidad que se puede producir con el etanol que se obtiene a partir del bagazo sobrante de los esquemas anteriores, con la electricidad que se genera a partir de la combustión directa del mismo, se corrobora que tal y como se demostró en la comparación de la cantidad de calor que se podía producir con ambos combustibles, con el bagazo se obtiene mucha más energía eléctrica y térmica, que con el etanol producido a partir de éste.
Si se toman dos casos de estudio de producción diversificada, el primero con producción de azúcar y de etanol a partir de miel final, y el segundo, con producción de azúcar y de etanol a partir de miel B y jugo de los filtros, tendremos como resultados los mostrados en los esquemas de las figuras 3 y 4, obtenidos en corridas del programa DAFLEX (Diversificación Azucarera Flexible) desarrollado en el ICIDCA sobre hoja de cálculo EXCEL [Díaz, et al., 2002]. Los esquemas anteriores se calcularon tomando como base los parámetros que se muestran en la tabla II.
Del análisis de ambos esquemas, y de los parámetros de operación de la tabla 2, se observa que las diferencias entre la energía eléctrica generada durante y después de zafra, así como en la energía consumida en los procesos de producción de azúcar y etanol, no son muy grandes; el segundo esquema (Fig. 4) vende 4,64 MWh más durante ambas etapas, que el primero (Fig. 3), en el que resulta mayor la electricidad vendida después de zafra (16,95 MWh), generada con el bagazo sobrante que se emplearía en la producción de etanol, si no se utilizara en la generación de electricidad. Por tanto, partiendo de una producción de 186 L de etanol por tonelada de bagazo con los procesos actuales de hidrólisis de biomasa, se simuló la generación de electricidad a partir del etanol obtenido con el bagazo sobrante en los dos esquemas anteriores, con las mismas condiciones de ambos, y que se presentan en las figuras 5 y 6, donde se observa que la cantidad de etanol producido en ambos esquemas se diferencia sólo en 2,24 t/día, que representan alrededor de 2 835 L de etanol más por día, pero la electricidad que se produce en ambos casos no difiere y es de 4,70 MWh.
En este caso, si se compara la electricidad que se puede producir con el etanol que se obtiene a partir del bagazo sobrante de los esquemas anteriores, con la electricidad que se genera a partir de la combustión directa del mismo, se corrobora que tal y como se demostró en la comparación de la cantidad de calor que se podía producir con ambos combustibles, con el bagazo se obtiene mucha más energía eléctrica y térmica, que con el etanol producido a partir de éste.
  Fig. 3. Esquema de producción diversificada. Miel final a etanol. |
  Fig. 4. Esquema de producción diversificada. Miel B y jugo de los filtros a etanol |
  Fig. 5. Generación de electricidad con el etanol producido con el bagazo sobrante en el esquema de miel final a etanol. |
  Fig. 6. Generación de electricidad con el etanol producido con el bagazo sobrante en el esquema miel final y jugo de los filtros a etanol. |
Tabla 2. Parámetros de la producción de azúcar
y etanol de los casos representados en las figuras 3 y 4
| Parámetro | Esquema 1 | Esquema 2 | Parámetro | Esquema 1 | Esquema 2 |
| Días de zafra | 180 | 180 | Consumo vapor proceso, t/t caña | 0,26 | 0,26 |
| Molienda real, t/día | 6 300 | 6300 | Índice general de vapor, t vapor/t bagazo | 7000 | 7000 |
| Caña molida, t/h | 262,5 | 262,5 | Número y capacidad de turbos | 1 de 15 MW | 1 de 15 MW |
| Bagazo en caña, kg/t caña | 285 | 285 | Eficiencia turbos, % | 0,80 | 0,80 |
| Cantidad de calderas | 1 | 1 | Consumo electricidad azúcar, MWh | 4,08 | 6,07 |
| Capacidad calderas, t/día | 100 | 100 | Consumo electricidad etanol, MWh | 0,79 | 0,79 |
| Presión de vapor vivo, kgf/cm2 | 42 | 42 | Bagazo disponible / calderas, t | 1 797,34 | 1 797,34 |
| Temperatura del vapor vivo, ºC | 400 | 400 | Bagazo/generación en zafra, t/día | 1 021,71 | 918,30 |
| Entalpía del vapor vivo, kCal/kg | 766,93 | 766,93 | Bagazo/generación después de zafra, t/día | 775,63 | 879,04 |
| Consumo vapor en turbogeneradores, kg/kW | 5 | 5 | Poder calorífico inferior del bagazo, kCal/kg | 1 850 | 1 850 |
| Presión vapor de escape, kgf/cm2 | 2,5 | 2,5 | Producción electricidad en zafra, MWh | 17,37 | 15,6 |
| Entalpía vapor de escape, kCal/kg | 648,85 | 648,85 | Producción electricidad después de zafra, MWh | 16,95 | 14,9 |
Los parámetros utilizados, sobre todo en cuanto a presión de vapor en la caldera y equipos de cogeneración, son aún modestos si se requiere potenciar la generación de electricidad. Si se realiza un análisis de la evolución técnica que ha sufrido la cogeneración en la industria azucarera, debido a los cambios de filosofía en cuanto a la disponibilidad de bagazo y su uso como fuente de energía, renovable y limpia, para la generación de electricidad, observamos que [Costa, 2008]:
 Fig. 7. Diagrama típico o tradicional de un ingenio azucarero. |
 Fig. 8. Diagrama típico optimizado de un ingenio azucarero. |
1. Antiguamente, el bagazo era considerado como un residual que ocasionaba un problema ambiental, por lo que debía ser quemado para resolver tal situación, y sólo se producía con él la electricidad y el vapor necesario para el proceso. Las calderas utilizadas eran de baja presión y temperatura, con una eficiencia pobre, al igual que las unidades de cogeneración que, en muchas ocasiones, no satisfacían todas las necesidades del ingenio azucarero. Por lo general, los motores mecánicos eran accionados con pequeñas turbinas de vapor, y sólo las bombas y otros equipos como las centrífugas, y otros, eran accionados por motores eléctricos (Fig. 7).
2. Posteriormente se optimiza el esquema anterior, produciéndose una generación de energía más eficiente, con una mejor relación presión/temperatura (Fig. 8), pero, sin embargo aún no bien optimizada y por debajo de las posibilidades reales. Las calderas de nueva generación tenían todavía una eficiencia media y subsistían aún demasiados motores mecánicos accionados con turbinas pequeñas de vapor, de baja eficiencia. No existía todavía un concepto definido de planta de generación de vapor y energía, pues la generación de electricidad no era todavía una necesidad.
3. Actualmente, la filosofía energética de la industria azucarera y de los derivados ha cambiado, debido al alza de los precios del petróleo, la necesidad de buscar fuentes alternativas de energía, limpias además, para evitar o disminuir la emisión de gases de efecto invernadero (Fig. 9). Por esta razón, la mayoría de los ingenios azucareros actuales presentan esquemas más eficientes de cogeneración, con mayores presiones, mayores eficiencias y con aporte de electricidad a la red. La producción de energía ha pasado a ser uno de los principales productos del ingenio azucarero, y los esquemas se caracterizan por [Costa, 2008]: Parámetros de alta presión y temperatura, con calderas de alta eficiencia
• Reemplazo de turbinas de vapor pequeñas por motores eléctricos con convertidor de frecuencia, por lo que se incrementa la eficiencia global de la planta
• La eficiencia es un objetivo fundamental en todo el ingenio azucarero. En algunos países se utiliza la paja y la punta de la caña como combustibles adicionales al bagazo Se utilizan equipos de alto comportamiento rendimiento y eficiencia
• Se realiza una evaluación técnica de los procesos de gasificación de la paja de la caña y el bagazo, para producir una migración a ciclo combinado.
2. Posteriormente se optimiza el esquema anterior, produciéndose una generación de energía más eficiente, con una mejor relación presión/temperatura (Fig. 8), pero, sin embargo aún no bien optimizada y por debajo de las posibilidades reales. Las calderas de nueva generación tenían todavía una eficiencia media y subsistían aún demasiados motores mecánicos accionados con turbinas pequeñas de vapor, de baja eficiencia. No existía todavía un concepto definido de planta de generación de vapor y energía, pues la generación de electricidad no era todavía una necesidad.
3. Actualmente, la filosofía energética de la industria azucarera y de los derivados ha cambiado, debido al alza de los precios del petróleo, la necesidad de buscar fuentes alternativas de energía, limpias además, para evitar o disminuir la emisión de gases de efecto invernadero (Fig. 9). Por esta razón, la mayoría de los ingenios azucareros actuales presentan esquemas más eficientes de cogeneración, con mayores presiones, mayores eficiencias y con aporte de electricidad a la red. La producción de energía ha pasado a ser uno de los principales productos del ingenio azucarero, y los esquemas se caracterizan por [Costa, 2008]: Parámetros de alta presión y temperatura, con calderas de alta eficiencia
• Reemplazo de turbinas de vapor pequeñas por motores eléctricos con convertidor de frecuencia, por lo que se incrementa la eficiencia global de la planta
• La eficiencia es un objetivo fundamental en todo el ingenio azucarero. En algunos países se utiliza la paja y la punta de la caña como combustibles adicionales al bagazo Se utilizan equipos de alto comportamiento rendimiento y eficiencia
• Se realiza una evaluación técnica de los procesos de gasificación de la paja de la caña y el bagazo, para producir una migración a ciclo combinado.
 Fig. 9. Diagrama de un ingenio azucarero actual. |
En la actualidad, dada la potencialidad de la industria azucarera, las plantas de azúcar y derivados se están convirtiendo en productores de energía, es decir, la energía pasa a ser un producto principal y deja de contemplarse como un subproducto. En los nuevos ingenios azucareros, o en aquellos que se remodelan sobre todo desde el punto de vista energético, se tienen en consideración para el diseño de la planta de cogeneración los siguientes factores [Costa, 2008; Herrera, 2010]:
• Utilización del bagazo sólo, o bagazo más paja de la caña como combustible.
• Parámetros de vapor. Altas presiones y temperaturas con bajo consumo de vapor por kW de electricidad producido.
• Reducción de consumos internos de vapor de proceso en todo el ingenio azucarero.
• Electrificación de los accionadores
• Conexión a la red pública
• Operación del ingenio azucarero sólo en zafra, o fuera de zafra, para producción de electricidad con el bagazo sobrante.
• Uso de nuevas tecnologías.La tendencia actual es la de aumentar la eficiencia de todos los equipos que intervienen en la producción y utilización de la energía, fundamentalmente la caldera y los turbogeneradores, lo que se resume según [Costa, 2008]:
• Parámetros de vapor por encima de 85 bares y 500 ºC.
• Producción de energía durante todo el año o la mayor parte de él.
• En cuanto a las turbinas se estimula el uso de una sola turbina de gran tamaño, de condensación-extracción y con álabes de reacción, en vez de dos unidades, una de contrapresión con extracción y otra de condensación, trabajando a 92 bares y 530 ºC.La siguiente tabla, compara los anteriores esquemas de cogeneración en cuanto a consumo específico de vapor/kW y energía eléctrica generada en MWh/año [Costa, 2008]:
Tabla 3. Comparación entre los diferentes esquemas de cogeneración
| Presión, bar | 21 | 42 | 65 | > 90 |
| Temperatura, ºC | 300 | 400 | 490 | > 500 |
| Consumo especifico, kg vapor/kW | 12,5 | 7,8 | 5,7 | 4,74 |
| Energía generada, MW/año | 38 400 | 61 500 | 84 200 | 101 300 |
| Incremento de generación, % | X | X + 60 | X + 200 | X + 260 |
No obstante, las bondades de la generación y cogeneración examinadas anteriormente con altas presiones y temperaturas de vapor, turbogeneradores de condensación extracción y gran tamaño, el rendimiento del ciclo Rankine es muy malo. Por ejemplo, con turbina y bomba de buenos rendimientos internos (cercanos a 85%), un ciclo de Rankine difícilmente supera 30%. Introduciendo mejoras como el sobrecalentamiento, el recalentamiento y la adecuada elección de las temperaturas y presiones de inicio y término de expansión, los ciclos de Rankine modificados pueden llegar a tener rendimientos cercanos a 40% [Monsalve, 2008].
Para obtener rendimientos más altos, se hace necesaria la incorporación de la tecnología de ciclo combinado, en la que se realiza la generación, mediante gas primero (turbina de gas), y mediante vapor en forma paralela e integrada, en una segunda etapa. De la misma manera, el gas de síntesis obtenido de la biomasa, podría ser tratado y convertido a etanol. Ambos procesos no están disponibles todavía a escala comercial, aún cuando la gasificación ya ha sido realizada a escalas piloto y demostrativa [Yanagihara].
Para obtener rendimientos más altos, se hace necesaria la incorporación de la tecnología de ciclo combinado, en la que se realiza la generación, mediante gas primero (turbina de gas), y mediante vapor en forma paralela e integrada, en una segunda etapa. De la misma manera, el gas de síntesis obtenido de la biomasa, podría ser tratado y convertido a etanol. Ambos procesos no están disponibles todavía a escala comercial, aún cuando la gasificación ya ha sido realizada a escalas piloto y demostrativa [Yanagihara].
 Fig. 10. Esquema y diagrama T vs. S para un ciclo combinado. |
Tomando la expresión de eficiencia térmica teórica máxima para cualquier máquina térmica, hacemos un análisis comparativo sencillo entre el ciclo Rankine y el ciclo combinado, partiendo de las siguientes condiciones: 1 100 ºC de temperatura de combustión del bagazo, en el ciclo Rankine se obtiene vapor en la caldera a 520 ºC, y se condensa a 70 ºC, temperatura de salida de la turbina de gas es de 520 ºC (se considera igual al del ciclo Rankine, lo cual no es cierto, pues no se pierde tanto calor en una turbina de gas), y 20% de pérdidas en la caldera de recuperación que genera vapor a 400 ºC, con 70 ºC en el vapor condensante, se tiene [AADECA, 1994; Lesme]:
• Ciclo Rankine: (1 - (70 + 273) / (520 + 273)) * 100 = 56,7%η
• Ciclo combinado: (1 - (550 + 273) / (1100+273)) + η (80 / 100)*((550 + 273) / (1 100 + 273))*(1-(70 + 273) / (400 + 273)) = [0,40 + 0,23] = 0,63 = 63,0% η
Del análisis anterior se desprende que aún imponiéndole al ciclo Bryton del ciclo combinado, las pérdidas de calor del ciclo Rankine, que no son ciertas, éste siempre tendrá como mínimo 10% de eficiencia por encima del Rankine. Un análisis más preciso se hubiera realizado con las expresiones de eficiencia de cada ciclo, con sus características. Por lo general, las diferencias entre ambos son muchísimo mayores.
Conclusiones
1. Inobjetablemente, el bagazo de la caña de azúcar tendrá siempre un valor de uso mucho mayor como combustible directo, que como materia prima para la producción de etanol.
2. La tendencia futura es la de lograr establecer, de manera económica y a mayor escala, la tecnología de gasificación de los materiales lignocelulósicos en general, y del bagazo de caña en particular, con la que se lograrán eficiencias mucho mayores en la producción de electricidad a partir de biomasa.
3. Sería de gran utilidad, aún con el ciclo Rankine mejorado (altas presiones y temperaturas, entre otras mejoras), adicionar los residuos de la cosecha cañera (RAC) tratados mecánicamente y mezclados con el bagazo, para incrementar la capacidad de generación de electricidad, y las ventas a la red durante y fuera de zafra.
4. El rendimiento actual de la tecnología de obtención de etanol de biomasa a partir de hidrólisis, tanto ácida como enzimática (186 L de etanol/t de bagazo), así como los rendimientos máximos posibles que se vislumbran con esta tecnología (~ 300 L de etanol/t de bagazo), no superan en valor energético las posibilidades de generación de energía eléctrica y térmica, a partir de la combustión directa de este material, con las tecnologías de cogeneración actuales, y mucho menos con la utilización de los ciclos combinados.
5. La generación de energía eléctrica a partir de bagazo, puede servir, además, para la venta de créditos de carbono, por evitar la emisión de gases de efecto invernadero, con lo que se logra la reevaluación de su uso como combustible limpio.
6. La gasificación del bagazo y la utilización de los ciclos combinados de generación y cogeneración, unido al establecimiento a escala comercial de la utilización del gas de síntesis para la producción de etanol, podrían, dada la eficiencia de ambos, permitir compromisos de generación eléctrica y de obtención de etanol, con balances económicos adecuados.
7. Independientemente a la afirmación anterior, sólo se podría pensar en la utilización del bagazo para la producción de etanol, en países con disponibilidad de otros recursos energéticos para la generación y cogeneración de electricidad, y con grandes reservas de hidrocarburos, que necesiten de grandes cantidades de etanol para la oxigenación de sus gasolinas, o su uso como combustible líquido para cumplimentar el Tratado de Kyoto, o de otros que, sin adecuadas reservas de combustible, posean grandes parques automotores. No obstante, tendrían que ser insuficientes las posibilidades de obtención de este combustible por los métodos tradicionales. Este caso podría ser por ejemplo, el de Venezuela, EE.UU. y Brasil, aunque éste último requiere mayor potencialidad hacia la generación de electricidad, que hacia la producción de etanol [BNDES, 2008].
Recomendaciones
1. Realizar estudios de factibilidad técnico-económicos que ayuden a establecer adecuadamente los usos más racionales del bagazo en cada caso particular.
2. Acelerar los estudios de ingeniería para la solución de los problemas que impiden el establecimiento a gran escala de la gasificación del bagazo, y de los ciclos combinados de generación y cogeneración.
3. Establecer los mecanismos para lograr la utilización de los RAC junto al bagazo, en la generación y cogeneración, lo que incrementará las capacidades actuales.
4. Para lograr la introducción adecuada de los RAC deberán estudiarse las distancias máximas de recolección de los mismos, que actualmente se establece para las condiciones cubanas en de 10 km del ingenio azucarero, aproximadamente; los tratamientos necesarios, así como el lugar de realización de los mismos para obtener las mejores relaciones costo/beneficio.
• Ciclo Rankine: (1 - (70 + 273) / (520 + 273)) * 100 = 56,7%η
• Ciclo combinado: (1 - (550 + 273) / (1100+273)) + η (80 / 100)*((550 + 273) / (1 100 + 273))*(1-(70 + 273) / (400 + 273)) = [0,40 + 0,23] = 0,63 = 63,0% η
Del análisis anterior se desprende que aún imponiéndole al ciclo Bryton del ciclo combinado, las pérdidas de calor del ciclo Rankine, que no son ciertas, éste siempre tendrá como mínimo 10% de eficiencia por encima del Rankine. Un análisis más preciso se hubiera realizado con las expresiones de eficiencia de cada ciclo, con sus características. Por lo general, las diferencias entre ambos son muchísimo mayores.
Conclusiones
1. Inobjetablemente, el bagazo de la caña de azúcar tendrá siempre un valor de uso mucho mayor como combustible directo, que como materia prima para la producción de etanol.
2. La tendencia futura es la de lograr establecer, de manera económica y a mayor escala, la tecnología de gasificación de los materiales lignocelulósicos en general, y del bagazo de caña en particular, con la que se lograrán eficiencias mucho mayores en la producción de electricidad a partir de biomasa.
3. Sería de gran utilidad, aún con el ciclo Rankine mejorado (altas presiones y temperaturas, entre otras mejoras), adicionar los residuos de la cosecha cañera (RAC) tratados mecánicamente y mezclados con el bagazo, para incrementar la capacidad de generación de electricidad, y las ventas a la red durante y fuera de zafra.
4. El rendimiento actual de la tecnología de obtención de etanol de biomasa a partir de hidrólisis, tanto ácida como enzimática (186 L de etanol/t de bagazo), así como los rendimientos máximos posibles que se vislumbran con esta tecnología (~ 300 L de etanol/t de bagazo), no superan en valor energético las posibilidades de generación de energía eléctrica y térmica, a partir de la combustión directa de este material, con las tecnologías de cogeneración actuales, y mucho menos con la utilización de los ciclos combinados.
5. La generación de energía eléctrica a partir de bagazo, puede servir, además, para la venta de créditos de carbono, por evitar la emisión de gases de efecto invernadero, con lo que se logra la reevaluación de su uso como combustible limpio.
6. La gasificación del bagazo y la utilización de los ciclos combinados de generación y cogeneración, unido al establecimiento a escala comercial de la utilización del gas de síntesis para la producción de etanol, podrían, dada la eficiencia de ambos, permitir compromisos de generación eléctrica y de obtención de etanol, con balances económicos adecuados.
7. Independientemente a la afirmación anterior, sólo se podría pensar en la utilización del bagazo para la producción de etanol, en países con disponibilidad de otros recursos energéticos para la generación y cogeneración de electricidad, y con grandes reservas de hidrocarburos, que necesiten de grandes cantidades de etanol para la oxigenación de sus gasolinas, o su uso como combustible líquido para cumplimentar el Tratado de Kyoto, o de otros que, sin adecuadas reservas de combustible, posean grandes parques automotores. No obstante, tendrían que ser insuficientes las posibilidades de obtención de este combustible por los métodos tradicionales. Este caso podría ser por ejemplo, el de Venezuela, EE.UU. y Brasil, aunque éste último requiere mayor potencialidad hacia la generación de electricidad, que hacia la producción de etanol [BNDES, 2008].
Recomendaciones
1. Realizar estudios de factibilidad técnico-económicos que ayuden a establecer adecuadamente los usos más racionales del bagazo en cada caso particular.
2. Acelerar los estudios de ingeniería para la solución de los problemas que impiden el establecimiento a gran escala de la gasificación del bagazo, y de los ciclos combinados de generación y cogeneración.
3. Establecer los mecanismos para lograr la utilización de los RAC junto al bagazo, en la generación y cogeneración, lo que incrementará las capacidades actuales.
4. Para lograr la introducción adecuada de los RAC deberán estudiarse las distancias máximas de recolección de los mismos, que actualmente se establece para las condiciones cubanas en de 10 km del ingenio azucarero, aproximadamente; los tratamientos necesarios, así como el lugar de realización de los mismos para obtener las mejores relaciones costo/beneficio.
domingo, 16 de noviembre de 2014
CALORIMETRÍA (2 DE BGU)
CALORIMETRÍA
La Calorimetría es la medida de la cantidad de calor que cede o absorbe un cuerpo en el curso de un proceso físico o químico.
CALOR
Es la Energía Térmica que se transfiere de un objeto a otro cuando entran en contacto mutuo, debido a una diferencia de temperaturas entre ellos. La dirección de la transferencia de la Energía Térmica es siempre desde la sustancia de mayor temperatura hacia la de menor temperatura (o sea desde la más caliente a la más fría). Cuando fluye calor entre dos objetos o sustancias que se encuentran unidas; se dice que están en CONTACTO TÉRMICO.
Mientras no hallan otros factores externos (el sistema sea cerrado) el calor perdido por el cuerpo A es igual al calor ganado en el cuerpo B.
OBSERVACIÓN: Es común, pero erróneo, pensar que la materia contiene calor. La materia contiene energía en diversas formas (Energía Interna), pero no contiene calor, ya que el calor es la energía que pasa entre dos objetos que se encuentran en contacto térmico debido a una diferencia de temperatura.
Cuando dos objetos se encuentran en contacto térmico, la temperatura del más caliente disminuye y la del más frío aumenta, hasta llegar ambos a la misma temperatura, es decir, quedan en EQUILIBRIO TÉRMICO. Al disminuir la temperatura de un cuerpo, la energía de sus moléculas también disminuye, y viceversa, si la temperatura aumenta, su Energía Interna también. El calor por lo tanto, antes de ser emitido es Energía Interna y después al ser transferido vuelve a ser Energía Interna. Expresado en forma de ecuación, queda: Q = calor transferido ∆E = cambio de energía interna
Como todo cambio ∆E es igual a la diferencia entre un estado final (E2) y uno inicial (E1), quedando:
PRINCIPIOS GENERALES DE LA CALORIMETRÍA
I. Siempre que entre varios cuerpos haya un intercambio de energía térmica, la cantidad de calor perdido por unos cuerpos es igual a la cantidad de calor ganada por los otros. II. La cantidad de calor absorbida o desprendida por un cuerpo es directamente proporcional a su variación de temperatura. Así, para elevar la temperatura de un cuerpo de 20°C se requiere el doble de cantidad de energía térmica que para elevarla a 10°C. III. La cantidad de calor absorbida o desprendida por un cuerpo es directamente proporcional a su masa. IV. Cuando varios cuerpos a temperaturas diferentes se ponen en contacto, la energía térmica se desplaza hacia los cuerpos cuya temperatura es más baja. El equilibrio térmico ocurre cuando todos los cuerpos quedan a la misma temperatura.
UNIDADES DE MEDIDA DEL CALOR
Siendo el calor una forma de energía, deben de medirse en las mismas unidades que ésta: joules, ergios, libras*pie ó Btu. Su relación de conversión es: Sin embargo, en la práctica se manejan otras unidades más adecuadas: CALORÍA (c) Es la cantidad de calor que se requiere para elevar la temperatura de 1 gramo de agua en 1°C. La relación entre calorías y joules es de: Existe también la Kilocaloría, o sea 1000 calorías (cantidad de calor necesaria para elevar en 1°C la temperatura de 1 Kg de agua). La Kilocaloría es la unidad en la que se mide el contenido energético de los alimentos y en la práctica se la llama usualmente Caloría, o Gran Caloría (con "C" mayúscula), para diferenciarla de la verdadera caloría (con "c" minúscula) llamada también pequeña caloría. NOTA: Recordar que la temperatura NO es una medida de la energía térmica total del cuerpo, es solo de su energía promedio. Es por esto que dos cuerpos pueden tener la misma temperatura pero distinta cantidad de energía interna. Ejemplo: Si se quiere hervir 10 litros de agua, se requiere 10 veces más energía que en el caso de un sólo litro, y aunque al final las temeperaturas sean las mismas (temperatura de ebullición del agua) debido a la diferencia de masas el consumo de energía es distinto.
CALOR ESPECÍFICO
Es la cantidad de calor que es necesario suministrarle a la unidad de masa de una sustancia para elevar su temperatura en 1°C. Cada sustancia tiene su propio valor de calor específico, por lo que cada uno requerirá distintas cantidades de calor para hacer que una misma cantidad de masa eleve su temperatura en 1°C. Para comprender esta definición, el significado del calor específico, se lo puede considerar como la "inercia térmica", recordando que el término de inercia se usa en la mecánica para denotar la resistencia que opone un objeto a los cambios en su estado de movimiento. De igual modo, el calor específico representa la inercia térmica porque denota la resistencia que opone una sustancia a los cambios de temperatura: Ejemplo: Si se calientan masas iguales de agua y de aluminio, el aluminio se calienta mucho más rapido que el agua; y si se les interrumpe el suministro de calor al mismo tiempo, el aluminio se enfría más rápido que el agua. En este caso, el agua presenta una mayor cantidad de calor específico que el aluminio, ya que requiere más calor para elevar su temperatura y se demora más tiempo en asimilar los cambios de temperatura (tiene más "inercia térmica"). FÓRMULA DEL CALOR ESPECÍFICO. La cantidad de calor Q que es necesario darle a una masa m de una sustancia para elevar su temperatura de T1 a T2 esta dada por la fórmula: De donde "ç" representa la constante de calor específico de la sustancia. Este valor es propio de cada material y se mide en: cal/(g*°C).
PROPAGACIÓN DEL CALOR
La transmisión del calor de una región a otra se puede efectuar sólo por alguna de estas tres formas: CONDUCCIÓN. Transferencia de calor a través de un cuerpo o entre dos cuerpos en contacto, sin que se desplacen las moléculas de los mismos. Ocurre sólo en los materiales sólidos. Ejemplo: Una barra de metal cuyo extremo se lo acerca a una llama, permite que fluya calor hasta su extremo opuesto. El desplazamiento de calor se realiza según la facilidad con lo que permita el material, de lo cual surge el concepto de Conductividad Térmica. CONVECCIÓN. Transferencia de calor entre dos partes de un cuerpo a causa del desplazamiento de sus moléculas. Ocurre sólo en los fluídos (líquidos y gases). El movimiento de las moléculas se origina por la diferencia de densidades que hay dentro de la sustancia, generando corrientes de convección desde las partes más calientes hacia las más frías en la masa del fluído. Ejemplo: Cuando se calienta un recipiente con agua, las moléculas del líquido que están en contacto con la zona caliente (llama) se mueven hacia la superficie donde se encuentran con el resto de moléculas más frías, haciendo que a su vez estas moléculas frías se desplacen hasta la zona de calor y comiencen el ciclo nuevamente. Este proceso dentro del líquido hace que el agua adquiera calor repetidamente, hasta alcanzar la temperatura suficiente de ebullición.
RADIACIÓN.
Transferencia de calor y energía de un cuerpo llamado foco a otro cuerpo distante, a través del VACÍO, es decir, sin la presencia de algún agente material o sustancia intermedia. Esta transferencia se logra gracias a que la energía se transporta por medio de Ondas Electromagnéticas las cuales pueden propagarse por el vacío sin ningún inconveniente. Ejemplo: Una bombilla emite luz y calor en forma de radiación. Esta radiación corresponde a: Ondas de Luz Visible (que nos permiten ver) y a las ondas infrarrojas (que nos dan la sensación decalor). Otras fuentes de luz como el Sol, aparte de las anteriores, también emite rayos X, microondas, ultravioleta, etc., las cuales no somos capaces de sentir, pero que sí lo pueden hacer aparatos e instrumentos apropiados.
Dar click sobre la imagen para ampliar información.
CONDUCTIVIDAD TÉRMICA
El calor se propaga en los materiales según la facilidad que éstos permitan hacerlo. En general, los materiales sólidos son los mejores conductores del calor (especialmente los metales), luego le siguen los líquidos y finalmente los gases, siendo éstos pésimos conductores del calor. A las sustancias que son malos conductores del calor se les llama aislantes térmicos, Ej: granito, madera, cueros, tejidos, etc.
La conductividad térmica de un material se halla por medio de la FÓRMULA DE FOURIER.
Si en una barra del material se tienen dos secciones iguales A1 y A2 (ambas de áreas A) a las temperaturas T1 y T2 respectivamente y separadas entre sí por una distancia d, entonces la cantidad de calor Q que pasa entre las dos secciones en un tiempo dado t, se obtiene por:
De donde "K" es la constante de conductividad térmica que es propia del material. Esta constante se mide en: cal/(m*seg*ºC).
NOTA: Aprende más con los siguientes videos.... click aquí.
|
LA MATERIA (1 DE BGU)
LA MATERIA Y SUS PROPIEDADES
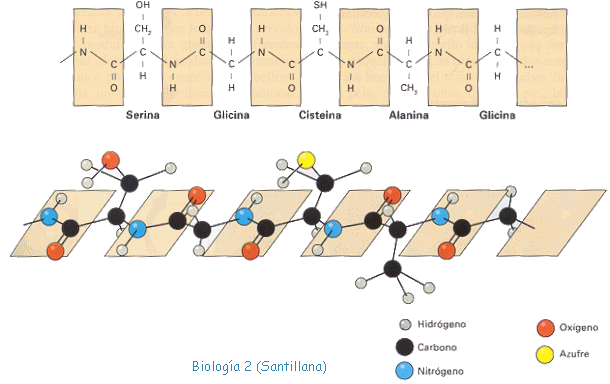
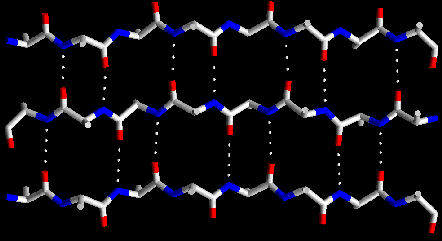
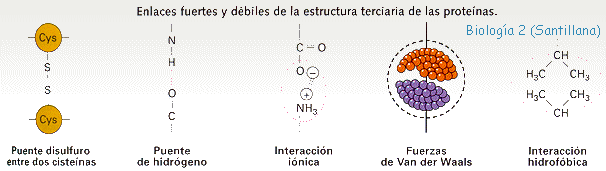
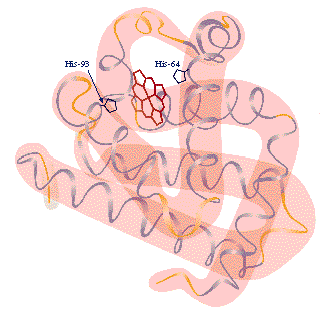
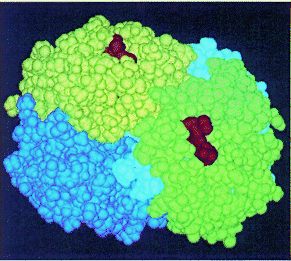
ESTRUCTURA DE PROTEÍNAS ( 3BGU)
 | 5.- Estructura tridimensional. |
domingo, 9 de noviembre de 2014
domingo, 2 de noviembre de 2014
Suscribirse a:
Entradas (Atom)