Ejercicios sobre las Leyes de los gases |
Ejercicio Nº 1
A presión de 17 atm, 34 L de un gas a temperatura constante experimenta un cambio ocupando un volumen de 15 L ¿Cuál será la presión que ejerce?
Solución:
Primero analicemos los datos:
Tenemos presión (P 1 ) = 17 atm
Tenemos volumen (V 1 ) = 34 L
Tenemos volumen (V 2 ) = 15 L
Claramente estamos relacionando presión (P) con volumen (V) a temperatura constante, por lo tanto sabemos que debemos aplicar la Ley de Boyle y su ecuación (presión y volumen son inversamente proporcionales):
Reemplazamos con los valores conocidos
Colocamos a la izquierda de la ecuación el miembro que tiene la incógnita (P 2 ) y luego la despejamos:
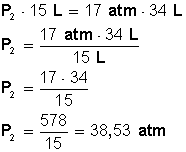
Respuesta:
Para que el volumen baje hasta los 15 L, la nueva presión será de 38,53 atmósferas.
Ejercicio Nº 2
¿Qué volumen ocupa un gas a 980 mmHg, si el recipiente tiene finalmente una presión de 1,8 atm y el gas se comprime a 860 cc?
Solución:
Analicemos los datos que nos dan:
Tenemos presión (P 1 ) = 980 mmHg
Tenemos presión (P 2 ) = 1,8 atm
Tenemos volumen (V 2 ) = 860 cc
Lo primero que debemos hacer es uniformar las unidades de medida.
Recuerda que la presión debe estar o en atmósferas (atm) o en milímetros de Mercurio (mmHg), pero no en ambas, y que el volumen debe estar en litros (L).
P 1 = 980 mmHg (lo dejamos igual)
P 2 = 1,8 atm lo multiplicamos por 760 y nos da 1.368 mmHg. Esto porque 1 atmósfera es igual a 760 mmHg
V 2 = 860 centímetros cúbicos lo expresamos en litros dividiendo por mil, y nos queda V 2 = 0,86 L (recuerda que un litro es igual a mil centímetros cúbicos).
Como vemos, de nuevo estamos relacionando presión (P) con volumen (V), a temperatura constante, por ello aplicamos la ecuación que nos brinda la Ley de Boyle (presión y volumen son inversamente proporcionales):
Reemplazamos con los valores conocidos
Ahora despejamos V 1
Respuesta:
A una presión de 980 mmHg dicho gas ocupa un volumen de 1,2 L (1.200 centímetros cúbicos).
Ejercicio Nº 3
A presión constante un gas ocupa 1.500 (ml) a 35º C ¿Qué temperatura es necesaria para que este gas se expanda hasta alcanzar los 2,6 L?
Solución:
Analicemos los datos:
Tenemos volumen (V 1 ) = 1.500 ml
Tenemos temperatura (T 1 ) = 35º C
Tenemos volumen (V 2 ) = 2,6 L
Lo primero que debemos hacer es uniformar las unidades de medida.
Recuerda que el volumen (V) debe estar en litros (L) y la temperatura (T) en grados Kelvin.
V 1 = 1.500 mililitros (ml), lo dividimos por 1.000 para convertirlo en 1,5 L
T 1 = 35º C le sumamos 273 para dejarlos en 308º Kelvin (recuerda que 0º C es igual a 273º K) (Nota: En realidad son 273,15, pero para facilitar los cálculos prescindiremos de los decimales).
V 2 = 2,6 L, lo dejamos igual.
En este problema estamos relacionando volumen (V) con temperatura (T), a presión constante, por lo tanto aplicamos la fórmula que nos brinda la Ley de Charles (volumen y temperatura son directamente proporcionales).
Reemplazamos con los valores conocidos
Desarrollamos la ecuación:
Primero multiplicamos en forma cruzada, dejando a la izquierda el miembro con la incógnita, para luego despejar T 2 :
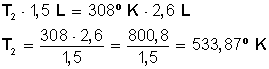
Entonces, para que 1,5 L expandan su volumen hasta 2,6 L hay que subir la temperatura hasta 533,78º Kevin, los cuales podemos convertir en grados Celsius haciendo la resta 533,87 − 273 = 260,87 º C.
Respuesta:
Debemos subir la temperatura hasta los 260,87º C.
Ejercicio Nº 4
¿Qué volumen ocupa un gas a 30º C, a presión constante, si la temperatura disminuye un tercio (1/3) ocupando 1.200 cc?
Solución:
Analicemos los datos:
Tenemos temperatura (T 1 ) = 30º C
Tenemos temperatura (T 2 ) = 30º C menos 1/3 = 20º C
Tenemos volumen (V 2 ) = 1.200 cc
Lo primero que debemos hacer es uniformar las unidades de medida.
Recuerda que el volumen (V) debe estar en litros (L) y la temperatura (T) en grados Kelvin.
T 1 = 30º C le sumamos 273 para dejarlos en 303º Kelvin (recuerda que 0º C es igual a 273º K)
T 2 = 20º C le sumamos 273 para dejarlos en 293º Kelvin (recuerda que 0º C es igual a 273º K) (Nota: En realidad son 273,15, pero para facilitar los cálculos prescindiremos de los decimales).
V 2 = 1.200 cc los dividimos por 1.000 para convertirlo en 1,2 L.
En este problema estamos relacionando volumen (V) con temperatura (T) a presión constante, por lo tanto aplicamos la fórmula que nos brinda la Ley de Charles (volumen y temperatura son directamente proporcionales).
Reemplazamos con los valores conocidos
Desarrollamos la ecuación:
Primero multiplicamos en forma cruzada, dejando a la izquierda el miembro con la incógnita, para luego despejar V 1 :
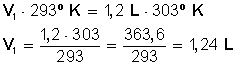
Respuesta:
A 30º C (303º K) el gas ocupa un volumen de 1,24 L (1.240 cc)
Ejercicio Nº 5
A volumen constante un gas ejerce una presión de 880 mmHg a 20º C ¿Qué temperatura habrá si la presión aumenta en 15 %?
Analicemos los datos:
Tenemos presión P 1 = 880 mmHg
Tenemos presión P 2 = 880 mmHg más el 15 % = 880 +132= 1.012 mmHg
Tenemos temperatura T 1 = 20º C
Lo primero que debemos hacer es uniformar las unidades de medida.
Recuerda que la temperatura (T) debe estar en grados Kelvin, y que la presión (P) puede estar solo en atm o solo en mmHg en una misma ecuación.
P 1 = 880 mmHg, lo dejamos igual
P 2 = 1.012 mmHg lo dejamos igual
T 1 = 20º C le sumamos 273 para dejarlos en 293º Kelvin (recuerda que 0º C es igual a 273º K) (Nota: En realidad son 273,15, pero para facilitar los cálculos prescindiremos de los decimales).
En este problema estamos relacionando presión (P) con temperatura (T) a volumen (V) constante, por lo tanto aplicamos la fórmula que nos brinda la Ley de Gay-Lussac (presión y temperatura son directamente proporcionales).
Reemplazamos con los valores conocidos
Desarrollamos la ecuación:
Primero multiplicamos en forma cruzada, dejando a la izquierda el miembro con la incógnita, para luego despejar P 2 :
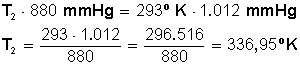
Respuesta:
Si aumentamos la presión en 15 % el gas quedará a una temperatura de 336,95º K, los cuales equivalen a 63,95º C. (336,95 − 273 = 63,95º C).
Ejercicio Nº 6
Cuando un gas a 85º C y 760 mmHg, a volumen constante en un cilindro, se comprime, su temperatura disminuye dos tercios (2/3) ¿Qué presión ejercerá el gas?
Solución
Analicemos los datos:
Tenemos presión P 1 = 760 mmHg
Tenemos temperatura T 1 = 85º C
Tenemos temperatura T 2 = 85º C menos 2/3 = 85 − 56,66 = 28,34º C
Lo primero que debemos hacer es uniformar las unidades de medida.
Recuerda que la temperatura (T) debe estar en grados Kelvin, y que la presión (P) puede estar solo en atm o solo en mmHg en una misma ecuación.
P 1 = 760 mmHg, lo dejamos igual
T 1 = 85º C le sumamos 273 para quedar en 358º K (recuerda que 0º C es igual a 273º K) (Nota: En realidad son 273,15, pero para facilitar los cálculos prescindiremos de los decimales).
T 2 = 28,34º C le sumamos 273 para quedar en 301,34º K
En este problema estamos relacionando presión (P) con temperatura (T) a volumen (V) constante, por lo tanto aplicamos la fórmula que nos brinda la Ley de Gay-Lussac (presión y temperatura son directamente proporcionales).
Reemplazamos con los valores conocidos
Desarrollamos la ecuación:
Primero multiplicamos en forma cruzada, dejando a la izquierda el miembro con la incógnita, para luego despejar P 2 :
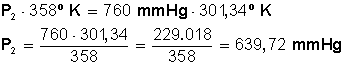
Respuesta
La presión baja hasta los 639,72 mmHg, equivalentes 0,84 atmósfera (1 atm = 760 mmHg)
TAREA
1. EN SU CUADERNO REALIZAR UN REFUERZO DE CADA LEY (Con la ayuda del texto. Pág. 120,121,122)
2. REALIZAR EN UNA HOJA PERFORADA UN EJERCICIO DE CADA LEY SOLO CAMBIANDO DE DATOS DE LOS EJERCICIOS PROPUESTOS
3. RECUERDE QUE TODAS LAS TAREAS TIENE QUE SER GUARDADAS EN UNA CARPETA PARA QUE EL PRIMER DÍA DE CLASE SEAN ENTREGADAS CONJUNTAMENTE CON SU CUADERNO PARA SER EVALUADAS.
SALUDOS CORDIALES A TODOS Y TODAS. RECUERDEN NO SALIR DE CASA. UN LINDO DÍA.
No hay comentarios:
Publicar un comentario