LISTADO DE DOCENTES PARA
LA ENTREGA DE SUS PORTAFOLIOS A SUS CORREOS
JORNADA NOCTURNA
UNIDAD
EDUCATIVA “OCTAVIO CORDERO PALACIOS”
N°
APELLIDOS Y NOMBRES
CELULAR
CORREO
1
Lcda. ASTUDILLO BEATRIZ
0990984289
2
Lcda. CASTILLO MARIA DOLORES. MSc
0999029802
3
Ing. CORDOVA MANUEL
0980210744
ocptareas@gmail.com
4
Lcdo. CHUMBAY WILFRIDO
0939823869
5
Lcdo. GUAZHAMBO ANGEL
0986159280
6
Lcdo. GUERRON WASHINGTON
0998089077
7
Arq. MINGA GARCIA ANDRES FELIPE
0995981909
9
Lcda. MOROCHO FAREZ DEYSI MARITZA
0989856677
10
Lcda. OCHOA CHICA SARA CARMITA
0980345995
12
Dra. OLMEDO CALVA LUPITA
0967553158
13
Ing. PERALTA BERMUDEZ DIEGO PATRICIO
MSc.
0998380848
14
Ing. QUITO PIEDRA JOSE. MSc
0980373282
15
Ing. VELEZ PEÑA CARLOS ALEJANDRO
0999425977
16
Psicóloga. JIMBO LILIANA
(DECE)
0983533121
17
SIEMPRE ADELANTE SOMOS OCTAVINOS DE CORAZÓN
SALUDOS CORDIALES
UNIDAD
EDUCATIVA “OCTAVIO CORDERO PALACIOS”
N°
APELLIDOS Y NOMBRES
CELULAR
CORREO
1
Lcda. ASTUDILLO BEATRIZ
0990984289
2
Lcda. CASTILLO MARIA DOLORES. MSc
0999029802
3
Ing. CORDOVA MANUEL
0980210744
ocptareas@gmail.com
4
Lcdo. CHUMBAY WILFRIDO
0939823869
5
Lcdo. GUAZHAMBO ANGEL
0986159280
6
Lcdo. GUERRON WASHINGTON
0998089077
7
Arq. MINGA GARCIA ANDRES FELIPE
0995981909
9
Lcda. MOROCHO FAREZ DEYSI MARITZA
0989856677
10
Lcda. OCHOA CHICA SARA CARMITA
0980345995
12
Dra. OLMEDO CALVA LUPITA
0967553158
13
Ing. PERALTA BERMUDEZ DIEGO PATRICIO
MSc.
0998380848
14
Ing. QUITO PIEDRA JOSE. MSc
0980373282
15
Ing. VELEZ PEÑA CARLOS ALEJANDRO
0999425977
16
Psicóloga. JIMBO LILIANA
(DECE)
0983533121
17
Distribución electrónica
Como resultado de los grandes esfuerzos realizados por muchos científicos, en la actualidad, la ciencia dispone de múltiples informaciones, comprobadas en la práctica, acerca de las leyes de distribución de los electrones en los átomos, partiendo del modelo de Bohr en la que señalaba la existencia de un núcleo formado por protones y neutrones, donde está concentrada la masa y la carga positiva del átomo. El electrón gira en órbitas circulares alrededor del núcleo, pero con algunas restricciones, como que solamente lo podía hacer en ciertas órbitas, cuya energía se encuentra cuantizada.
Por niveles electrónicos
Asumiendo el modelo de Bohr, los electrones se distribuyen en los átomos formando capas alrededor del núcleo que reciben el nombre de capas electrónicas o también niveles energéticos. Todos ellos forman la envoltura electrónica que rodea al núcleo. Mientras mayor número de capas electrónicas posea un átomo, mayor será la distancia que separa al núcleo de los electrones más externo.
Cada una de las capas electrónicas posee distinto contenido o nivel de energía y se encuentran a diferentes distancias del núcleo, de forma tal que la capa electrónica de menor nivel de energía será la más próxima al núcleo y las de mayores niveles energéticos se encontrarán más alejadas de éste. A medida que los electrones se encuentren en una capa electrónica alejada del núcleo con gran contenido energético estarán más débilmente unidos a éste. .
Los diferentes niveles energéticos toman valores enteros a partir de 1; por lo que el valor del primero, o sea, para el que corresponde a la capa más próxima al núcleo es 1, el que corresponde a la segunda capa es 2, etcétera. Estos niveles se representan también, a veces, por las letras K,L,M,N,O,P y Q.
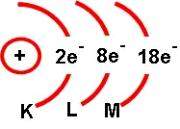
Aunque de acuerdo con la concepción actual del átomo no es posible representarlo gráficamente, desde un punto de vista pedagógico es conveniente tener una representación visual, que, aunque no corresponda exactamente a la realidad, tampoco la contradiga, en la que se utilizan esquemas como el mostrado a continuación:
El núcleo se puede representar con un pequeño círculo donde se señalan tanto protones como indica su número atómico, y tantos neutrones como indica la diferencia entre el índice de masa y el número atómico. La envoltura se puede representar por arcos de circunferencia con centro en el núcleo. Cada arco corresponde a un nivel de energía y en el se coloca un número que indica los electrones que existen en ese nivel.
Se ha podido determinar el número máximo de electrones que pueden agruparse en los distintos niveles de energía y tenemos:
Al analizar bien lo anterior, se observa que cada nivel puede contener un número máximo de electrones igual a 2n2, donde n puede ser 1,2,3, etc., según el nivel energético. Aunque esto no quiere decir que siempre tendrán ese número máximo de electrones. Así, se tendrá que: .
El máximo número de electrones en la penúltima capa es 18 Si la penúltima capa no está completa, el máximo número de electrones en la capa más externa es 2
Particularidades de los electrones de los últimos niveles y la tabla periódica
Puesto que la capa K solo puede alojar dos electrones quedará completa en el gas inerte Helio. Después de este, se va llenando la capa L, con un electrón en el Litio hasta ocho en el Neón, cuya situación es análoga a la del Helio. Con dos en la capa K y ocho en la L quedan ambas capas totalmente ocupadas, mientras que las exteriores a ellas continúan vacías por completo.
El Neón es también un gas inerte, lo que significa que tras un período o ciclo de ocho átomos reaparece la propiedad de la inercia química. En los ocho átomos siguientes, los electrones se adicionan a la tercera capa, M, aumentando gradualmente su número desde el Sodio hasta ocho en el Argón. Cabria suponer que este elemento, número 18 no debería ser un gas inerte, ya que de acuerdo al diagrama de los niveles energéticos la capa M puede admitir hasta diez electrones más, esto es, 18; pero la observación nos dice que el Argón es un gas inerte, y que por tanto, la tercera capa debe considerarse completa cuando contenga ocho electrones.
Desde el punto de vista químico los niveles más externos, y fundamentalmente el último, son los más importantes; pues ellos:
- Permite explicar la recurrencia periódica de los elementos, sus propiedades dependen esencialmente del número de electrones que contiene el nivel energético más externo.
Por ejemplo, en el caso del Litio este posee un electrón en la capa mas externa (nivel L), y lo mismo sucede con el Sodio, aunque se encuentra el electrón en el nivel M. En la tabla periódica los elementos químicos con propiedades semejantes se sitúan uno debajo de otros, lo que equivale a reunir en un grupo aquellos átomos que contienen igual número de electrones en su nivel energético más externo
- Son los electrones que actúan cuando se produce una reacción química.
Por ello con frecuencia los átomos también pueden representar electrónicamente, de un modo simplificado, indicando sólo los electrones del nivel más externo por medio de puntos junto a su símbolo, a esta representación se le llama representación electrónica simplificada o estructura electrónica simplificada. Estas representaciones son llamadas estructuras de Lewis.
Por ejemplo:
El modelo de Bohr no puede ser aplicado a átomos más complejos o a moléculas, manifestado en la distribución electrónica por niveles de energía. Es un modelo semiclásico, porque supone la cuantización de la energía del átomo, pero describe el movimiento del electrón en forma de una trayectoria circular alrededor del núcleo, tal como la física clásica de Newton describe el movimiento de los planetas alrededor del sol y permite calcular la posición de estos en cualquier instante de tiempo.
De la evidencia acumulada del estudio de diversos fenómenos a la escala atómica surgió el convencimiento de que la física de Newton no era aplicable a los electrones y a las demás partículas pequeñas. A partir de ello se plasmó una nueva visión del mundo físico: la mecánica cuántica.
Por la notación nlx
Actualmente para saber a dónde se localizan los electrones en el modelo atómico cuántico se utiliza la configuración electrónica.
Las configuraciones electrónicas de los átomos de los diferentes elementos químicos se expresan convencionalmente en función de los números cuánticos. La manera más útil y empleada de representar la distribución de los electrones en los orbitales de los distintos niveles, es la representada simbólicamente por la notación nlx, donde n representa en forma de número el nivel principal l, el subnivel en forma de letra(s,p,d,f) y x, el número total de electrones en este subnivel. Si todos los niveles electrónicos del átomo se designan de esta forma, la suma de los valores de x debe darnos el número atómico Z.
Reglas para el llenado de los orbitales:
Para acomodar correctamente los electrones en el Modelo Atómico de la Mecánica Cuántica Ondulatoria, existen reglas fundamentales para el llenado de los orbitales:
1.- Principio de exclusión de Pauli afirma que dos electrones no pueden tener en ningún sistema orbital (entiéndase átomo) iguales sus cuatro números cuánticos; en otras palabras, dos electrones pueden tener el mismo conjunto de números cuánticos, si tienen distintos los números que corresponden al espin (sus espines han de estar orientados en sentidos opuestos).
2.- La regla de Hund o de máxima multiplicidad dice que, al llenar orbitales de energía equivalente, los espines de los electrones permanecen desapareados, si es posible; en otras palabras, que el llenado de los orbitales se realiza de tal manera, que el espín resultante sea el máximo.
3.- Principio de Aufbau, de Edificación Progresiva o de Construcción: Los orbitales se llenan según sus energías relativas, empezando por aquellos de menor energía.
Se puede, ahora, deducir las configuraciones electrónicas de los átomos en su estado fundamental sin más que suponer que estos pueden construirse por sucesiva adición de electrones, ocupando estos primeramente los niveles energéticos más bajos disponibles y entrando en los niveles más altos únicamente cuando los más bajos estén llenos. Este es el llamado principio de Aufbau o de construcción, que no es más que el cumplimiento de las reglas planteadas anteriormente.
Existe una regla práctica que nos permite encontrar el orden energético ascendente de los distintos orbitales y que es útil para representar las configuraciones electrónicas a partir del número atómico o carga nuclear.Esta regla se llama regla de las diagonales.
El orden en que van siendo ocupados los orbitales de los distintos subniveles se obtiene siguiendo la dirección de las diagonales de arriba hacia abajo ordenadamente, para ello se debe seguir la flecha del esquema de la derecha, comenzando en 1s; siguiendo la flecha se podrá ir completando los orbitales con los electrones en forma correcta.
Se pueden aplicar las reglas anteriores cuando se representa la distribución electrónica por niveles, subniveles y orbitales a partir del número atómico.
Para graficar la configuración electrónica existen cuatro modalidades, con mayor o menor complejidad de comprensión, que son:
Configuración estándar
Se representa la configuración electrónica considerando la configuración estándar (la que se obtiene del rayado electrónico) . Recordar que los orbitales se van llenando en el orden en que aparecen.
Aplicando el mencionado cuadro de las diagonales la configuración electrónica estándar, para cualquier átomo, es la siguiente:
1s22s22p63s23p64s2 3d10 4p6 5s2 4d1 0 5p6 6s2 4f14 5d10 6p67s2 5f14 6d10
Los valores que se encuentran como superíndices indican la cantidad máxima de electrones que puede haber en cada subnivel (colocando sólo dos en cada orbital de los subniveles).
Configuración condensada
Los niveles que aparecen llenos en la configuración estándar , se pueden representar con un gas noble (elemento del grupo VIII A ) , donde el número atómico del gas , coincida con el número de electrones que llenaron el último nivel. Los gases nobles son (He , Ne, Ar , Kr , Xe y Rn ).
Configuración desarrollada
Consiste en representar todos los electrones de un átomo , empleando flechas para simbolizar el spin de cada unos. El llenado se realiza respetando el principio de exclusión de Pauli y la Regla de máxima multiplicidad de Hund
Configuración semidesarrollada
Esta representación es una combinación entre la configuración condensada y la configuración desarrollada . Aquí solo se representan los electrones del último nivel de energía.
TAREA
ES UNA HOJA PERFORADA REALICE DIEZ EJEMPLOS DE DISTRIBUCIÓN ELECTRÓNICA, COMENZANDO DESDE EL BERILIO Y SUMANDO CINCO

No hay comentarios:
Publicar un comentario