¿Qué es la meiosis?
Se denomina meiosis a una de las formas en que se dividen las células, caracterizada por dar lugar a células hijas genéticamente distintas a la célula madre que las originó. Este tipo de división celular es clave para la reproducción sexual, ya que a través de la meiosis los organismos producen sus gametos o células sexuales. El nuevo individuo resultante de la unión de dos gametos (uno masculino y uno femenino) tendrá un material genético distinto al de los parentales, que surge de la combinación de estos.
La meiosis consiste en la división de una célula diploide (2n), es decir, provista de dos juegos de cromosomas para dar lugar a cuatro células haploides (n), provistas de un único juego de cromosomas, es decir, la mitad de la carga genética de la célula inicial.
En los animales y el ser humano la mayor parte de las células del cuerpo son diploides y se las llama células somáticas. Únicamente en el tejido germinal se encuentran células especiales que dan lugar a través de la meiosis a células haploides. Estas células haploides son los gametos o células reproductivas que intervienen en la reproducción sexual, es decir, son los espermatozoides (gametos masculinos) y los óvulos (gametos femeninos). Cuando un espermatozoide y un óvulo se fusionan entre sí durante la fecundación, cada uno de ellos aporta la mitad de la carga genética del nuevo individuo que se forma como resultado de esta unión. Así, ambos juegos haploides de cada gameto se combinan para formar un conjunto diploide completo, que es el genoma del nuevo individuo recientemente formado.
Como vimos, la meiosis es un proceso imprescindible previo a la reproducción sexual, dado que durante este proceso se forman los gametos. Sin embargo, la meiosis también forma parte de ciclos de vida complejos, en algas, hongos y otros eucariontes sencillos, para lograr cierta alternancia generacional, reproduciendo sus células de modo sexual y asexual en distintas etapas.
La meiosis fue descubierta en el siglo XIX por el biólogo alemán Oscar Hertwig (1849-1922), a partir de sus estudios con huevos de erizo de mar. Desde entonces sucesivas investigaciones han contribuido para entender este proceso con mayor profundidad y para comprender su vital importancia en la evolución de las formas superiores de vida.
Ver además: Célula eucariota
Fases de la meiosis
La meiosis es un proceso complejo que involucra dos fases diferenciadas: meiosis I y meiosis II. Cada una de ellas está compuesta por diversas etapas: profase, metafase, anafase y telofase. Ello amerita un estudio más detallado:
- Meiosis I. Primera división celular de la diploide (2n), conocida como reductiva, pues resulta en células con la mitad de la carga genética (n).
- Profase I. El primer paso consiste en la preparación del ADN para devenir dos conjuntos distintos, por lo que el material genético se entrecruza y surge en la célula una suerte de línea divisoria.
- Metafase I. Los cromosomas se ubican en el centro de la célula (ecuador) y empiezan a separarse. La repartición genética al azar ya se ha llevado a cabo.
- Anafase I. Cada ristra de ADN tiende a un polo de la célula, formando dos polos haploides (n).
- Telofase I. La membrana plasmática se separa y se da origen a dos células haploides.
- Meiosis II. Conocida como fase duplicativa, pues se asemeja a la mitosis: se forman dos individuos enteros duplicando el ADN.
- Profase II. Las células haploides creadas en la meiosis I condensan sus cromosomas y rompen la envoltura nuclear.
- Metafase II. Al igual que antes, los cromosomas tienden hacia la mitad de la célula, preparándose para una nueva división.
- Anafase II. El material genético tiende a separarse y migrar hacia los polos de la célula, alistando el nuevo proceso de división celular.
- Telofase II. Las membranas celulares se separan nuevamente y dan como resultado cuatro células haploides (n), cada uno con una distribución distinta del código genético completo del individuo.
Meiosis y mitosis
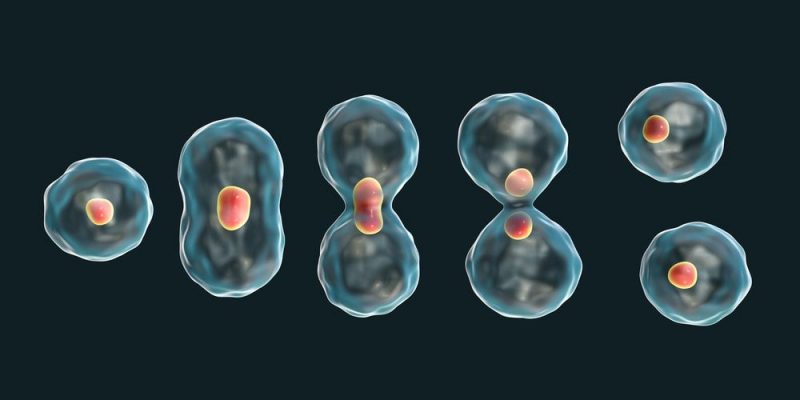
Las diferencias entre mitosis y meiosis son varias:
- La mitosis está asociada a la reproducción asexual. La mitosis consiste en la división de una célula original para formar dos células hijas genéticamente idénticas. La mitosis es utilizada como mecanismo en los distintos tipos de reproducción asexual, en los cuales un organismo produce “clones” celulares, sin añadir variedad al pozo genético. La meiosis, en cambio, es un proceso requerido en la preparación para la reproducción sexual, y a diferencia de la mitosis, permite una alta recombinación genética.
- La mitosis está asociada a procesos de desarrollo y crecimiento. Los organismos pluricelulares utilizan el mecanismo de la mitosis para mantener y renovar sus estructuras corporales. Así, este tipo de división celular permite agregar células nuevas durante el desarrollo y crecimiento del individuo y sustituir las células viejas y gastadas a lo largo de la vida del organismo.
- La mitosis crea dos células hijas. Ambas diploides e idénticas. La meiosis, en cambio, produce cuatro células descendientes, pero todas haploides y distintas entre sí y a la célula madre.
- La mitosis preserva el ADN. La mitosis es un mecanismo de preservación del material genético intacto (aunque pueden ocurrir mutaciones al azar durante el proceso), mientras que la meiosis lo somete a un proceso de recombinación en el cual pueden ocurrir errores, pero que también enriquece el genoma y permite la creación de cadenas particularmente exitosas. La meiosis es en algún punto gran responsable de la variación genética entre individuos.
TAREA
ESCRIBA LAS FASES DE LA MEIOSIS CON UNA EXPLICACIÓN PEQUEÑA