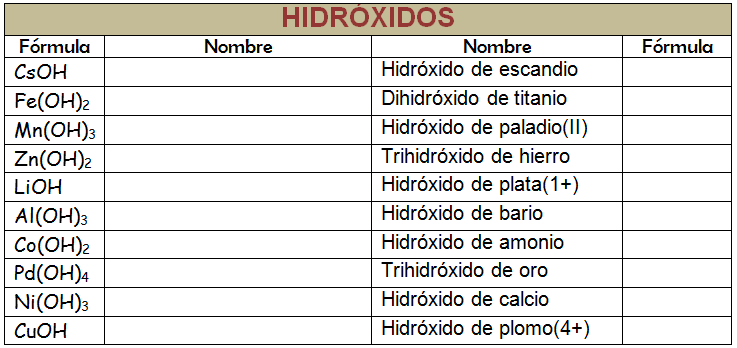
Ley de Boyle-Mariotte – Ejercicios Resueltos
Es muy probable que al leer el enunciado citado arriba, no lo entiendas del todo, y te doy la razón, está confuso en principio, pero aquí te diré que nos quiere dar a entender.Vamos a establecer matemáticamente el enunciado.
Despejando, de tal forma que nos quede la unidad en el miembro derecho, tendremos algo así.
Introduciendo la constante de proporcionalidad, nos queda que:
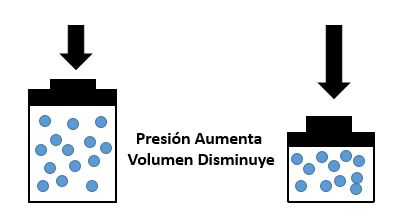
Ahora, si queremos ver los cambios que experimentará un gas, comúnmente se hace en un estado inicial y final, por lo que la expresión matemática o fórmula de Boyle-Mariotte queda de la siguiente forma.
Dónde
🔹 Fórmula de la Ley de Boyle – Mariotte
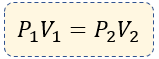
🔸 Ejemplos resueltos de la ley de Boyle-Mariotte
Solución:Lo primero que vamos analizar para la resolución del problema, son nuestros datos, saber que tenemos y que nos hace falta.
Por lo que podemos observar el problema nos pide el volumen final es decir
Despejando >>
Por lo que nuestro volumen final es de
Con esto podemos concluir que mientras la presión bajó el volumen aumentó.
No es difícil analizar dichos problemas, veamos otro ejemplo.
Solución:
Al igual que el problema anterior lo que necesitamos es conocer nuestros datos, sin los datos no podemos hacer absolutamente nada, ahora hagamos de nuevo un listado de nuestros datos.
Observamos que lo que nos falta es la presión final, por lo que vamos a despejar
Despejando >>
Sustituyendo nuestros datos.
Tenemos que 1.25 atm. es la presión final de lo que nos pide nuestro problema, sin embargo el mismo problema dice que tenemos que convertir las unidades de presión, en este caso atmósferas a mm de Hg para ello haremos una regla de tres.
Si 1 atm equivale a 760 mm de Hg, 1.25 atm ¿a cuántos mm de Hg equivaldría?
1 atm ———– 760 mm de Hg
1.25 atm ———— x mm de Hg
por lo que 950 mm de Hg es la presión final obtenida en un recipiente de 3 litros.
¿Aún no quedó claro?
📃 Ejercicios para Practicar de la Ley de Boyle Mariotte
Para aprender mucho mejor el tema de la Ley de Boyle – Mariotte, es importante resolver más ejercicios y comprender los problemas para entender que variable tenemos que despejar y poder resolver sin ningún problema. Los siguientes ejercicios son explicados paso a paso en su solución, pero primero resuélvalos usted en su cuaderno o libreta. 😊👇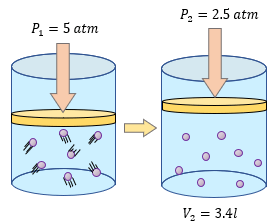
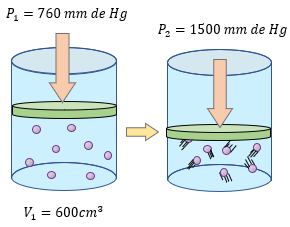
👉
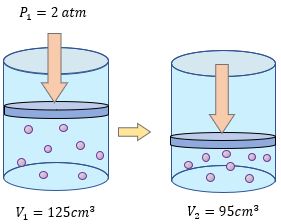
Problema 5.- Un gas recibe una presión de 2 atmósferas y ocupa un volumen de 125 cm³, calcular la presión que debe soportar para que su volumen sea de 95 cm³